Радиационная стерилизация медицинских изделий, фармацевтических. Методы, средства и режимы стерилизации Лучевая стерилизация медицинских изделий
Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
2.6.4. ИСТОЧНИКИ
ИОНИЗИРУЮЩЕГО ИЗЛУЧЕНИЯ
В НАРОДНОМ ХОЗЯЙСТВЕ
3.5.4. СТЕРИЛИЗАЦИЯ
Общие требования
к технологическому регламенту радиационной
стерилизации изделий медицинского назначения
однократного применения
Руководство
Р 2.6.4/3.5.4.1040-01
Минздрав России
Москва 2001
Общие требования к технологическому регламенту радиационной стерилизации изделий медицинского назначения однократного применения: Руководство. - М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2001.
1. Разработано организационно-методическим Центром Минздрава России «Радиационная стерилизация медицинских изделий» (Пономарев В.Н., Молин А.А., Драбкин Ю.А., Калашников В.В.).
3. Утверждено и введено в действие Главным государственным санитарным врачом Российской Федерации - Первым заместителем Министра здравоохранения Российской Федерации 28 мая 2001 г.
4. Введено впервые.
УТВЕРЖДАЮ
Главный государственный
санитарный врач Российской
Федерации - Первый заместитель
Министра здравоохранения
Российской Федерации
Г.Г. Онищенко
2.6.4. ИСТОЧНИКИ ИОНИЗИРУЮЩЕГО ИЗЛУЧЕНИЯ В НАРОДНОМ ХОЗЯЙСТВЕ
3.5.4. СТЕРИЛИЗАЦИЯ
Общие требования к технологическому регламенту радиационной стерилизации изделий медицинского назначения однократного применения
Руководство
Р 2.6.4/3.5.4.1040-01
1. Область применения
1.1. Настоящее руководство устанавливает общие требования к построению, изложению, согласованию и утверждению технологических регламентов радиационной стерилизации изделий медицинского назначения однократного применения, производимых отечественными предприятиями.
1.2. Настоящее руководство предназначено для предприятий и организаций Российской Федерации, осуществляющих разработку, производство и радиационную стерилизацию изделий медицинского назначения однократного применения, независимо от их формы собственности и ведомственной принадлежности.
1.3. Руководство разработано в соответствии с «Основами законодательства Российской Федерации об охране здоровья граждан», федеральным законом «О санитарно-эпидемиологическом благополучии населения», Положением о Министерстве здравоохранения Российской Федерации, Положением о государственной санитарно-эпидемиологической службе и Положением о государственном санитарно-эпидемиологическом нормировании.
2. Нормативные ссылки
2.1. «Основы законодательства Российской Федерации об охране здоровья граждан» от 22 июля 1993 г. № 5487-1 (Ведомости съезда народных депутатов Российской Федерации и Верховного Совета Российской Федерации, 1993, № 33, ст. 1318).
2.2. Федеральный закон «О санитарно-эпидемиологическом благополучии населения» (Собрание законодательства РФ № 14, от 05.04.99, ст. 1650).
2.3. Положение о Министерстве здравоохранения Российской Федерации, утвержденное постановлением Правительства Российской Федерации от 3 июня 1997 г. № 659 с изменениями и дополнениями (Собрание законодательства Российской Федерации, 1997, № 23, ст. 2691, № 51 ст. 5809, 1999, № 47 ст. 5706).
2.4. Положение о государственной санитарно-эпидемиологической службе и Положение о государственном санитарно-эпидемиологическом нормировании (утвержденные Постановлением Правительства РФ от 24.07.00 № 554) (Собрание законодательства Российской Федерации, 2000, № 31, ст. 3295).
3. Цели и задачи
Руководство Р 2.6.4/3.5.4.1040-01 создано с целью нормативного обеспечения радиационной стерилизации, являющейся финишной технологической операцией производства изделий медицинского назначения однократного применения категории «стерильно».
Руководство разработано для решения задачи установления единых требований к порядку разработки, построению, изложению и оформлению технологического регламента радиационной стерилизации изделий медицинского назначения однократного применения, что, в свою очередь, позволяет унифицировать требования надежности, санитарно-гигиенического контроля и безопасности производства.
4. Термины и определения
В этом разделе приведены наиболее употребляемые термины и определения.
4.1. Радиационная стерилизация медицинских изделий
Необратимая инактивация микроорганизмов всех видов, находящихся на всех стадиях развития, на и в изделиях медицинского назначения, осуществляемая с помощью ионизирующего излучения.
4.2. Технологический процесс радиационной стерилизации
Совокупность технологических операций и последовательность их выполнения при осуществлении радиационной стерилизации медицинских изделий, как часть процесса производства стерильных изделий.
4.3. Технологический регламент радиационной стерилизации
Нормативный документ, устанавливающий методы, технические средства, и нормы процесса радиационной стерилизации изделий медицинского назначения, обеспечивающие безопасность ведения работ и достижение требуемых технико-экономических показателей.
4.4. Радиационная установка для стерилизации
Техническое устройство, обеспечивающее безопасное и надежное проведение процесса стерилизации, имеющее в своем составе источник ионизирующего излучения, транспортную систему и приводные механизмы управления источниками, систему обеспечения и контроля безопасности.
4.5. Радионуклидная установка
Радиационная установка, в которой источником ионизирующих излучений является закрытый радионуклидный источник.
4.6. Электрофизическая радиационная установка
Радиационная установка, в которой источником ионизирующих излучений является электрофизический (генерирующий) источник ионизирующего излучения.
В тексте документа используются следующие сокращения:
PC - радиационная стерилизация;
РД - радиационная деконтаминация;
ТР - технологический регламент;
РТУ - радиационно-технологическая установка;
ОМЦ PC - организационно-методический центр «Радиационная стерилизация медицинских изделий» Минздрава России.
5. Общие положения
5.1. Технологический регламент радиационной стерилизации - нормативный документ, устанавливающий метод, технические средства, условия и порядок технологического процесса радиационной стерилизации изделий медицинского назначения однократного применения в целях обеспечения санитарно-гигиенических условий, безопасности ведения работ и качества изделий, соответствующего требованиям нормативно-технической документации на продукцию, а также достижения оптимальных технико-экономических показателей процесса радиационной стерилизации.
5.2. Технологический регламент радиационной стерилизации используют при отработке технологии и при осуществлении промышленного процесса радиационной стерилизации изделий медицинского назначения.
5.3. Технологический регламент на стадии отработки технологии радиационной стерилизации имеет срок действия не более 1 года. Его составляют на основе данных проектной и иной технической документации на процесс стерилизации данного вида изделий, а также на основании данных эксплуатации аналогичных существующих производств с учетом вида источника излучения и технологических особенностей радиационно-технологической установки (РТУ) стерилизации. Освоение производства считается законченным, когда достигнуто стабильное выполнение требований нормативно-технической документации на продукцию, а также достигнуты воспроизводимость технологического процесса по мощности и основным технико-экономическим показателям производства.
5.4. Технологический регламент действующего процесса радиационной стерилизации составляют с учетом изменений и дополнений, принятых при освоении производства. Установленный срок действия регламента производства - 5 лет. Порядок внесения, согласования и утверждения изменений в регламент тот же, что и для самого регламента.
5.5. Технологический регламент допускается составлять на стерилизацию однородного типа продукции, например, на шприцы однократного применения разных типоразмеров и емкости.
5.6. Технологический регламент составляют только для конкретной РТУ с определенным типом источника излучения, соответствующего ГОСТам 27632, 27212 и 30392. Запрещается переносить условия процесса, определяемые технологическим регламентом на конкретной РТУ, на процесс стерилизации на иной РТУ с другими характеристиками источника и технологической оснастки.
6. Требования к построению технологического регламента
Нормы и требования, включаемые в технологические регламенты радиационной стерилизации медицинских изделий, должны соответствовать требованиям действующих стандартов, нормативно-технических документов на продукцию, правил и норм Минздрава России, Госатомнадзора, отраслевых и межотраслевых правил и норм техники безопасности, санитарных правил обеспечения радиационной безопасности и норм радиационной безопасности, а также других нормативных документов, в части организации и проведения радиационной стерилизации медицинских изделий.
6.1.1. Технологический регламент процесса радиационной стерилизации должен состоять из следующих разделов:
· характеристика конечной продукции производства;
· технологическая схема производства;
· спецификация оборудования;
· характеристика сырья и материалов;
· описание технологического процесса;
· нормы технологического процесса;
· неполадки в работе и способы их устранения;
· переработка и обезвреживание отходов производства;
· контроль производства и управление технологическим процессом;
· техника безопасности, пожарная безопасность и производственная санитария;
· перечень производственных инструкций;
· технико-экономические нормативы.
6.1.2. Характеристика конечной продукции процесса должна содержать:
· наименование продукции;
· категорию действующей нормативно-технической документации, номер действующих ГОСТов, технических условий, инструкций и т.п.;
· регистрационный номер Минздрава России;
· основное назначение продукции, краткое описание внешнего вида, потребительских свойств;
· основные микробиологические характеристики изделия (инициальная контаминация, требования к стерильности после обработки в технологическом цикле стерилизации);
· требования к упаковке, маркировке, транспортированию, условиям хранения и срокам годности изделия;
· объемную плотность упаковки с медицинскими изделиями (для РТУ с ускорителями электронов).
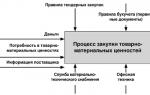
6.1.3. Технологическую схему процесса выполняют в виде блок-схемы отображающей последовательность выполнения работ в процессе радиационной стерилизации. Обозначение стадий: ВР - вспомогательные работы, ТП - стадии основного технологического процесса.
6.1.4. В раздел «Спецификация оборудования» включают перечень, тип, обозначение конструкторско-технической документации всего оборудования, используемого в технологическом процессе:
· источника излучения;
· транспортного устройства;
· контрольно-измерительной аппаратуры;
· дозиметрического оборудования;
· вспомогательного оборудования;
· оборудования, обеспечивающего радиационную безопасность процесса.
Для источника излучения указывают: тип радионуклида и его активность для РТУ с изотопным источником, или мощность источника излучения, ток пучка, частоту импульсов и т.д. для РТУ с ускорителем электронов.
6.1.5. В раздел «Характеристика сырья и материалов» включают наименование и тип всех вспомогательных материалов, используемых для упаковки, крепежа, изоляции и т.п., а также индикаторных и дозиметрических материалов для контроля облучения.
6.1.6. Раздел «Описание технологического процесса» излагают последовательно по стадиям с учетом проведения операций, в точном соответствии с технологической схемой производства, причем описание должно обеспечить всеми необходимыми данными воспроизводимость процесса и безопасность работ.
6.1.7. В описании подраздела «Входной контроль» предусматривают описание процедур проверки поступающей на стерилизацию продукции:
· соответствия требованиям нормативно-технической документации на продукцию по форме, упаковке, габаритам, весу, маркировке;
· наличия сопроводительной документации на партию изделий;
· необходимости дополнительных мер контроля нестерильной продукции, например, по параметру инициальной контаминации изделий.
6.1.8. В описании операций по выводу РТУ на режим указывают порядок работ, обеспечивающий параметры процесса, определенные регламентом, в т.ч. источника излучения, транспортного устройства, контрольно-измерительной аппаратуры и защитных устройств.
6.1.9. Описание порядка загрузки изделий на транспортное устройство, подающее их в камеру облучения, дают в подразделе «Загрузка изделий».
6.1.10. Порядок проведения облучения для обеспечения стерилизующей дозы на каждом изделии, не допускающим превышение максимально допустимой дозы, соблюдение и контроль за режимом работы источника излучения и транспортного устройства описывают в подразделе «Стерилизация».
6.1.11. Порядок выгрузки изделий, проведения контрольных дозиметрических измерений и контроля за индикаторами дозы описывают в подразделе «Выгрузка изделий».
6.1.12. В подразделе «Приемочный контроль» дают описание контроля за правильностью облучения изделий, процедуры оформления необходимой документации, отправки изделий предприятию-изготовителю или иному заказчику.
6.1.13. В разделе «Нормы технологического процесса» приводят по операциям процесса нормы технологического режима, необходимые элементы работы для их обеспечения и контрольные точки режима, в т.ч. допустимого диапазона доз облучения изделий, которые контролируются персоналом РТУ и которые обеспечивают качество и безопасность процесса стерилизации. Раздел выполняют в виде таблицы (приложение 4).
6.1.14. В разделе «Неполадки в работе и способы их устранения» дают описание возможных неполадок (отклонений от нормального хода технологического процесса), возникающих в ходе технологического процесса, приводят меры предупреждения и перечень мероприятий, их устраняющих, или перечень инструкций, где указан порядок проведения этих мероприятий.
6.1.15. В разделе «Переработка и обезвреживание отходов производства» указывают перечень и краткую санитарно-гигиеническую характеристику отходов процесса стерилизации, в т.ч. газообразных, порядок их обезвреживания, методы устранения.
6.1.16. Контроль производства и управление технологическим процессом описывают в отдельном разделе регламента, где указывают перечень контрольных точек, приведенных в разделе «Нормы технологического режима», методы их контроля на всех стадиях работы РТУ - выводе на режим, облучении, выводе из эксплуатации, а также перечень процедур, проводимых на каждой стадии процесса для поддержания оптимального технологического режима, обеспечивающего высокое качество стерилизации.
Порядок проверки правильности контроля должен регламентироваться документами, приведенными в разделе «Перечень производственных инструкций».
6.1.17. В разделе «Техника безопасности, пожарная безопасность и производственная санитария» дают в виде таблиц:
· описание аварийных состояний процесса, способов их предупреждения и устранения, порядок повторного пуска установки;
· пожаро- и взрывоопасные и токсичные свойства сырья, готового продукта и отходов производства радиационной стерилизации, с учетом требований ГОСТа 12.1.004 «Пожарная безопасность. Общие требования» и ГОСТа 12.1.044 «Пожаровзрывоопасность веществ и материалов»;
· категории по взрывопожароопасности, классы производственных помещений и наружных установок, категории и группы радиационно-опасных и взрывоопасных мест, установленных по НПБ 105-95/ МВД;
· перечень наиболее опасных мест процесса, меры предосторожности для персонала;
· санитарно-гигиеническую характеристику производственных процессов, составленную на основе гигиенического заключения на производство радиационной стерилизации медицинских изделий (в соответствии с приказом Минздрава России от 20.07.98 № 217);
· требования по предупреждению микробной загрязненности продукции в процессе стерилизации, при хранении и транспортировании;
· средства групповой и индивидуальной защиты работников РТУ и вспомогательного персонала.
6.1.18. В перечне производственных инструкций приводят инструкции по эксплуатации источников, транспортного устройства, дозиметрической аппаратуры, а также по технике безопасности.
6.1.19. В разделе «Технико-экономические нормативы» указывают ежегодные нормы расхода технологических материалов и энергозатрат (воды, электроэнергии, сжатого воздуха, инертных газов и т.п.), принципы определения стоимости процесса и нормативы экономической эффективности его проведения.
6.2. Оформление регламента
6.2.1. Регламент печатают с одной стороны листа через 1, 5 интервала на бумаге формата А4 по ГОСТу 2.301. Листы нумеруют порядковым номером и брошюруют.
Ошибки, опечатки в тексте не допускаются. Оформление регламента допускается с использованием компьютеров или другой техники.
6.2.2. Текст регламента должен отвечать требованиям ГОСТа 2.105, быть предельно ясным и лаконичным.
6.2.3. Разделы регламента нумеруют цифрами, а наименования разделов записывают прописными буквами. Наименование подразделов записывают строчными буквами без нумерации и выделяют или подчеркивают.
6.2.4. Нумерацию пунктов производят арабскими цифрами по разделам, например: 1.1, 1.2., ... 1.1.1., 1.1.2., где на первом месте указан номер раздела, на втором - номер пункта, на третьем - подпункта. Цифры разделяют точкой.
6.2.5. Титульный лист является первым листом регламента и оформляется в соответствии с приложением . За титульным листом должен следовать лист с заглавием «Содержание регламента».
6.2.6. Последний лист технологического регламента подписывается основными разработчиками регламента, с указанием должности и наименования отдела (лаборатории).
6.2.6.1. Последний лист регламента подписывают: начальник отдела (лаборатории), разработавшего регламент, руководитель группы разработчиков регламента, непосредственные разработчики регламента, руководитель микробиологической службы, ответственный за технику безопасности в организации.
7. Порядок разработки, согласования и утверждения регламента
7.1. Технологические регламенты радиационной стерилизации медицинских изделий разрабатываются предприятием радиационной стерилизации в соответствии с настоящим руководством. Разрешается разработка технологического регламента организационно-методическим Центром Минздрава России «Радиационная стерилизация медицинских изделий» (ОМЦ PC).
Технологические регламенты стерилизации являются неотъемлемой частью комплекта технической документации на медицинское изделие, выпускаемое по категории «Стерильное».
7.2. Разработанный технологический регламент утверждается предприятием-производителем медицинского изделия, подвергаемого радиационной стерилизации. Один экземпляр утвержденного технологического регламента передается предприятию-производителю изделия.
7.3. По поручению Департамента Минздрава России научно-техническую экспертизу проектов технологических регламентов осуществляет ГНЦ - Институт биофизики.
7.4. Проекты технологических регламентов радиационной стерилизации изделий медицинского назначения должны проходить научно-техническую экспертизу на соответствие требованиям действующих нормативных документов, стандартов, правил и норм.
7.5. Эксперты несут ответственность за:
· объективность, компетентность, достоверность и обоснованность проводимой экспертизы;
· независимость и гласность принимаемых решений и выдаваемых рекомендаций;
· соблюдение при рассмотрении документов и материалов конфиденциальности в отношении вопросов, защищаемых авторским правом и правом коммерческой тайны.
7.6. Научно-техническая экспертиза осуществляется на договорной основе и завершается согласующей подписью руководителя экспертной организации на титульном листе регламента. Срок экспертизы не должен превышать одного месяца.
7.7. Технологические регламенты утверждаются руководителем предприятия радиационной стерилизации после утверждения предприятием-производителем изделий и согласования экспертной организацией.
7.8. Технологические регламенты радиационной стерилизации по поручению Департамента Минздрава России регистрирует ГНЦ - Институт биофизики.
Обозначение регламента должно состоять: из типа регламента ТР - технологический регламент; номера регламента, присваиваемого при регистрации: - 001, 002 ...; типа процесса - PC - радиационная стерилизация, РДК - радиационная деконтаминация; года утверждения регламента - 2000-00, 2001-01 ...
Пример: ТР-003 PC-00.
7.9. Регистрация утвержденных технологических регламентов производится в специальном регистрационном журнале.
7.10. Технологические регламенты после их утверждения и регистрации представляются по одному экземпляру по месту регистрации в ГНЦ - Институт биофизики.
Регистрационные журналы и регламенты хранятся отдельно от другой технической документации на правах служебных документов.
7.11. Изменения к регламенту оформляются в виде ведомости изменений с приложением пояснительной записки. Согласование, утверждение, регистрация изменений технологических регламентов и их хранение производится в том же порядке, что и для самих регламентов.
7.12. Срок действия технологического регламента подтверждается каждые 5 лет. Подтверждение действия регламента оформляется протоколом, который согласуется и утверждается в том же порядке, что и сам регламент.
Приложение 1
(обязательное)
Форма титульного листа технологического регламента радиационной стерилизации изделий медицинского назначения однократного применения
ТЕХНОЛОГИЧЕСКИЙ РЕГЛАМЕНТ
на
радиационную стерилизацию
(название медицинского изделия, его обозначение, марка)
(название предприятия-производителя медицинского изделия, его обозначение)
(Обозначение регламента и его регистрационный номер, например, ТР-001 РС-01)
Срок действия регламента до «___» _______________ 200__ г.
СОГЛАСОВАНО
Руководитель (Директор, заместитель) ГНЦ
Институт биофизики
__________________ /Ф. И. О./
«_____» ____________ 200___ г.
Москва 200 ____ г.
Приложение 2
Образец описания технологического регламента
Технологический регламент
на радиационную
стерилизацию (наименование изделия)
однократного применения по ТУ (№
ТУ)
производства (наименование предприятия-производителя)
Разработан предприятием радиационной стерилизации медицинских изделий однократного применения - (наименование предприятия радиационной стерилизации).
Радиационная стерилизация указанных выше (наименование изделий) в соответствии с настоящим нормативным документом проводится только на технологической установке предприятия радиационной стерилизации, физические параметры и технические характеристики которой определены настоящим технологическим регламентом.
Осуществление радиационной стерилизации (наименование изделия) однократного применения на установках радиационной стерилизации других предприятий с иными физическими параметрами и техническими характеристиками по данному технологическому регламенту запрещается.
2. Технологическая схема процесса
3. Спецификация оборудования
4. Характеристика сырья и материалов
5. Описание технологического процесса
8. Переработка и обезвреживание отходов процесса
9. Контроль производства и управление технологическим процессом
11. Перечень производственных инструкций
1. Характеристика конечной продукции процесса
Изделия на радиационную стерилизацию (PC ) поступают в транспортной таре - (описание транспортной тары с указанием размеров, в мм) соответствующими (или несоответствующими) ряду размеров, предусмотренных ГОСТ (например, ГОСТ 21140). В таре содержатся изделия (подробно описываются вид индивидуальной упаковки изделия с указанием упаковочных материалов, их ГОСТ, ТУ, наличие или отсутствие групповой упаковки, их количество в транспортной таре, количество изделий в групповой упаковке и т.п.)
Соответствующая масса нетто единицы транспортной тары с (наименование изделия): до (указывается предельная масса тары с изделиями) кг.
Объемная плотность для коробки с (наименование изделий) - до (предельная плотность) г/см 3 .
Это условие обязательно при использовании для радиационной стерилизации ускорителей электронов типа (указывается тип ускорителя) с энергией (указывается энергия) в режиме (указывается режим одно- или двухстороннего) облучения.
Таблица 1
Характеристики стерильной продукции
|
Наименование показателя |
Продукция / характеристика, норма |
|
(наименование продукции) |
|
|
Внешний вид |
(описывается вид изделия в упаковке) |
|
Объемная плотность упаковки (коробка), г/см 3 |
|
|
Микробиологические нормативы по группам |
|
|
Масса нетто единицы потребительской тары, г |
|
|
Масса брутто единицы транспортной тары с изделиями, кг |
|
|
Размеры транспортной тары, мм |
Стерилизация (название изделия) проводится с использованием (указывается тип) источников излучения - (указывается конкретно установка с источником излучения). Процесс является экологически чистым, т. к. при его проведении не происходит образования радиоизотопов, т.е. не имеет место наведенная радиоактивность и изделия не загрязняются радионуклидами.
2. Технологическая схема процесса радиационной стерилизации (название изделия) однократного применения по ТУ (№ ТУ) производства (наименование предприятия-производителя)
Схема № 1
3. Спецификация оборудования
Таблица 2
|
Наименование |
Количество единиц |
Техническая характеристика |
Документация |
|
Радиационно-технологическая установка (РТУ) в составе: |
|||
|
Источник излучения |
|||
|
Транспортное устройство |
|||
|
Контрольная аппаратура |
|||
4. Характеристика сырья и материалов
(наименования вспомогательных материалов, дозиметрических средств, индикаторов дозы и т.п.)
5. Описание технологического процесса
Стадия ВР.1. Входной контроль
Перед началом техпроцесса необходимо убедиться, что предназначенные для PC (наименование изделий) по физико-механическим параметрам, упаковке и фасовке соответствуют техническим условиям, (см. разд. настоящего регламента), и на них имеется утвержденная соответствующим порядком документация.
К радиационной стерилизации допускаются изделия, прошедшие государственную регистрацию в Минздраве России в установленном порядке.
Партия (наименование изделий) должна иметь сопроводительный документ, в котором указывается государственный регистрационный номер изделия, номер партии и количество изделий, форма потребительской тары, а также результаты определения инициальной контаминации (ИК) изделий (при их наличии).
Описывается процедура контроля данных по инициальной контаминации, соответствующих выходных данных изделия после стадии упаковки, наличие их на этикетке.
Описываются процедуры входного контроля массы упаковки, порядка укладки и т.п. параметров транспортной тары.
Описывается процедура контроля дозиметрических средств и индикаторов дозы.
Стадия ВР.2. Вывод установки на режим
Описывается порядок ввода источников в активное состояние, или порядок приведения ускорителей электронов в рабочий режим.
Описывается процедура контроля дозы в рабочем режиме установки, проведение контрольного измерения дозы в контрольной точке.
Описывается процедура установки контрольных дозиметров, подачи транспортной тары с изделиями на транспортное устройство и подачи их в зону облучения.
Стадия ТП.1. Стерилизация
Описывается процедура стерилизации с указанием параметров доз облучения, режимов работы РТУ, режимов облучения изделий - кратность проходов, ориентация упаковок с изделиями, порядок дозиметрического контроля в ходе стерилизации.
Данные режима облучения и контроля дозы заносить в контрольный журнал оператора.
При выявлении сбоя режима ускорителя процесс PC прекратить, повторить операции, описанные в разделе . Вывод установки на режим, после чего продолжить облучение.
После окончания полного цикла облучения снять коробки с транспортного устройства проверить наличие индикаторов (или детекторов рабочих дозиметров при контрольных измерениях дозы) на коробках, проверить соответствие цвета индикатора установленному контрольному цвету. Коробки, на которых установлено это соответствие, считать прошедшими радиационную стерилизацию и складировать в хранилище готовой продукции. Снять детекторы рабочих дозиметров с коробок (при контрольных измерениях дозы) и провести измерения дозы (указать каким образом, с использованием каких средств). Методику дозиметрического контроля осуществлять в соответствии с ГОСТом 30392-95.
Стадия ВР.5. Приемочный контроль
Определить коробки, прошедшие стерилизацию, в соответствии с п. ; определить значения дозы излучения по показаниям рабочих дозиметров. Данные контрольных измерений дозы занести в журнал оператора.
Коробки, не прошедшие облучение или недооблученные (что следует установить по показаниям рабочих дозиметров - значение дозы меньше значения стерилизующей дозы) направлять на повторное облучение дозой, равной разнице между стерилизующей дозой и дозой, определенной на поверхности ящика, после полного цикла облучения.
По результатам облучения составить протокол стерилизации партии изделий по установленной форме. Протокол представить предприятию-производителю по завершению процесса PC партии изделий.
Предприятие-производитель контролирует по представленным протоколам качество стерилизации и несет ответственность за качество (название изделий), стерилизованных радиационным методом с регламентированной дозой.
6. Нормы технологического процесса
|
Наименование операции |
Наименование элементов работы |
Технологические показатели |
|
ВР.1. Входной контроль |
||
|
ВР.2. Вывод установки на режим |
||
|
ТП.1. Стерилизация |
||
|
ВР.4. Выгрузка изделий |
||
|
ВР.5. Приемочный контроль |
7. Неполадки в работе и способы их устранения
Неполадки в работе (название РТУ) - устраняются в соответствии с (наименование инструкции или другого документа).
Неполадки в работе транспортного устройства (наименование устройства) устраняются в соответствии с Инструкцией по эксплуатации и техническими условиями (№ № документов).
8. Переработка и обезвреживание отходов
(Приводится характеристика отходов производства и их вредного воздействия на окружающую среду и человека).
Выбросы в атмосферу и сточные воды не содержат (если содержат то какие) вредных и токсичных веществ. Оценочные (по экспериментальным данным) выбросы по озону составляют: - максимальная разовая приземная концентрация озона в атмосферном воздухе составляет (указываются нормативы для конкретной установки) мг/м 3 , при допустимой разовой (концентрация указывается) мг/м 3 (с вероятностью (указывается цифра) %).
Среднесуточная допустимая концентрация озона в атмосфере населенных пунктов (указывается в соответствии с ПДВ - 83 мг/м 3).
9. Контроль и управление технологическим процессом
Входной контроль провести в соответствии с разделом .
Текущий дозиметрический контроль. Проводить согласно ГОСТ Р 30392-95 при совместной работе (указывается тип РТУ) и транспортного устройства. Контролируемые параметры (приводятся конкретные цифры параметров, которые необходимо контролировать при проведении процесса PC ).
ТП.1. Облучение изделий
Контролируются параметры при работе (указывается тип РТУ) косвенно, исходя из поглощенной дозы в контрольной точке тары с изделиями после облучения, равной (указывается значение величины дозы) кГр. Контроль провести аналогично разделу .
ВР.4. Выгрузка изделий
Объект контроля - цветовой индикатор дозы (указать тип) (или дозиметр (указать тип) при контрольных измерениях дозы). Периодичность контроля - индикатор дозы на каждом ящике с двух сторон, детектор рабочего дозиметра - согласно требованиям ГОСТ 30392-95 «Изделия медицинского назначения. Методика дозиметрии при проведении процесса радиационной стерилизации».
Контролируемый параметр - цвет индикатора. Метод определения цвета - визуально, сравнением с контрольным цветом (возможно по цветовой шкале).
Данные измерений пересчитывают в дозу по калибровочной таблице. Данные заносят в журнал стенда.
ВР.5. Приемочный контроль
Приемочный дозиметрический контроль - аналогично п. . Запись о дозиметрическом контроле (в частности, величине средней стерилизующей дозы) вносится в протокол, который подписывается дозиметристом и оператором.
Запись о дозе стерилизации вносится в протокол стерилизации на (наименование изделия), прошедшие PC.
10. Техника безопасности, пожарная безопасность и производственная санитария
10.1. Аварийные состояния процесса и способы их устранения и предупреждения
10.2. Пожаро- и взрывоопасные и токсичные свойства сырья, полупродуктов, готового продукта и отходов процесса
Наименование вещества: (указать пожароопасные, токсичные вещества в ходе процесса);
Сырье - нестерильные (название изделий); продукт процесса PC - стерилизованные (название изделий) - нетоксичны.
10.4. Перечень наиболее опасных мест процесса
|
Наименование |
Вид опасности |
Меры предосторожности |
10.5. Санитарная характеристика производственных процессов (ПП)
10.6. Средства индивидуальной защиты работающих
11. Перечень производственных инструкций
|
Наименование инструкций и документов |
Обозначение |
12. Технико-экономические нормативы
Стоимость радиационной стерилизации (наименование изделий) определена в (указать параметр стоимости в абсолютном или относительном выражении), исходя из стоимости 1 часа облучения на ускорителе, включая стоимость электроэнергии, воды, аренды помещений и других накладных расходов, а также производительности установки при облучении данного вида продукции.
РАЗРАБОТАНО (указать организацию-разработчик ТР)
Подписи разработчиков:
Руководитель подразделения, разработавшего ТР
Ответственный за разработку
Руководитель микробиологической службы
Ответственный за ТБ
Библиографические данные
1. Порядок разработки, экспертизы, утверждения, издания и распространения нормативных и методических документов системы государственного санитарно-эпидемиологического нормирования: Сборник. Р.1.1.001-1.1.005-96: Минздрав России. - М., 1998.
12. Нормы радиационной безопасности (НРБ-99): Гигиенические нормативы. ГН 2.6.1.758-99 .
13. Определение индивидуальных эффективных и эквивалентных доз и организация контроля профессионального облучения. Общие требования: Методические указания. МУ 2.6.1.016-2000. - М., 2000.
14. Дозиметрический контроль внешнего профессионального облучения. Общие требования: Методические указания. МУ 2.6.1.25-2000. - М., 2000.
15. МИ 2548-99 ГСИ. Установки радиационно-технологические с радионуклидными источниками излучения для стерилизации изделий медицинского назначения. Методика аттестации.
16. МИ 2549-99 ГСИ. Установки радиационно-технологические с ускорителями электронов для стерилизации изделий медицинского назначения. Методика аттестации.
ПРОМЫШШННЫЕ УСТАНОВКИ ДЛЯ РАДИАЦИОННОЙ СТЕРИЛИЗАЦИИ
МЕДИЦИНСКИХ ИЗДЕЛИЙ
В.Б.Осипов, С.В.Мамиконян, Ь. М. Т е р е н т ь е в, Ю.С.Горбунов,
А.А.Кудрявцев, Г. Д. С т е п а н о в, И.И.Сарапкин, Н.Г.Коньнов,
Б.М.Ванюшкин, СЮ.Крылов, Э. С. К о р ж е н е в с к и й, В.М.Левин,
В.А.Глухих, В.И.Мунтян, Ю.И.Сафонов
Радиационная стерилизация медицинских изделий (в частности,
из полимерных материалов) исторически явилась одной из первых областей промышленного освоения радиационной технологии " * ". На современном этапе в мире функционирует более трех десятков крупных радиационных установок данного назначения. При этом идут двумя путями, т. е. с использованием в качестве мощного источника ионизирующего излучения как электронных ускорителей (наиболее широко в С А Ш и Дании), так и радиоизотопных источников гамма-излучения. Показательны данные Э.Э.Фаулера, приведенные им в обзорном докладе на 1У Ееневской конференции " ~ ". Из 50 крупных радиационных установок, созданных га последние годы в С А для реализации различных радиаШ ционных процессов, 40 базируются на ускорителях электронов, а 10 имеют облучатели из кобальта-60 с суммарной активностью ~ 9 Мкц (ИЛИ эквивалентной мощностью *~ 130 к з г). Это примерно в 3 раза больше того, что С А имели к моменту проведения Ш Женевской конфеШ ренции. Общая мощность ВД ускорителей » 710 квт, чтопримерно в 5 раз превышает мощность кобальтовых установок. Потребности С А в Ш промышленной радиационной стерилизации медицинских инструментов и медикаментов обеспечиваются тремя автоматизированной центрам, в
59 которых сосредоточено по нескольку гамма-установок.
Большими мощностями располагает радиационная промышленность Франции (~ 26 т.Мрад/день)*}. Радиационную стерилизацию осуществляют две компании, использующие гамна-установки на кобальте-60 и цезии-137. На одной из заводов в качестве источника излучения используется линейный ускоритель электронов годностью 10 квх. Потребность в медицинских изделиях быстро растет благодаря расширяющемуся применению полимерных материалов при изготовлении изделий. Радиационной стерилизации стали подвергать перчатки, трубки, шприцы, системы для переливания крови, а также скальпели, медикаменты, посуду, одежду, белье и т. д. В частности, обычная дневная выработка ва заводе "Капри" (Франция) шприцев для подкожного впрыскивания - продукции, пользующейся сейчас большим спросом на европейском рынке, составляет на этом предприятии 3 млн.шг* (для шприцев емкостью Z мл) и 0,5 млн.шт. (при емкости 20 мл).
Дания располагает значительным числом электронных ускорителей с общей мощностью ~ 800 квх. Примерно на 80% всех установок проводится коммерческое облучение медицинских изделий с целый радиационной стерилизации. Для большей надежности радиационной стерилизации на датских ускорителях стерилизующая доза повышена до 3,5-4,0 Мрад.
Таким образом, как следует из состояния работ в данной области, в ряде развитых капиталистических стран радиационная стерилизация в целом перестала быть ааучно-технической проблемой и переживает ныне период становления в индустриальную отрасль медицинской промышленности.
Решение и развитие данной проблемы в нашей стране началось несколько лет назад. Основанием к этому послужили результаты отечестй
М)своенная на 1971г. мощность, а проектная мощность этих существующих радиационных производств - 70 т.Мрад/день ™"
60 венных исследований, показавшие, что радиационная стерилизация обеспечивает:
Гарантированную высокую степень бактерицидности различных стерилизуемых изделий (в т. ч. и объемную, которая иногда недостижима при использовании других известных методов стерилизации);,
Возможность стерилизации термолабилъных пластических материалов и изделий из них различной конфигурации;
Безопасность применения аростерилизованных изделий и материалов;
Сохранение достигнутой степени стерильности за счет обработки изделий в герметичных упаковках того или иного вида, являющихся "прозрачными" для ионизирующего излучения при стерилизации и "непрозрачными" для проникновения через них микроорганизмов после процесса стерилизации и при последующем хранении;
Возможность организации непрерывно-поточной (автоматизированной) линии радиациогаой обработки в условиях заводского производства соответствующих изделий в упакованном виде;
Конкурентоспособность метода по сравнению с другими методами стерилизации при его внедрении в промышленное производство пекоторых изделий медицинского назначения.
Имевшая место за рубежом и в СССР дискуссия по вопросу применения типа источников ионизирующего излучения (электронные ускорители или радиоизотопные источники гамма-излучения) не выявила доминирующего положения какого-либо источника. Поэтому в СССР разработки установок данного назначения выполняются с использованием как источников гамма-излучения (кобальта-60), так и электронных ускорителей ". Это согласуется с современными тенденциями, вытекающими также из анализа материалов 1У Женевской конференции, а именно созданием установок по радиационной стерилизации с массовым применением для
61 обработки изделий гамма-излучения радиоизотопных: источников (большей частью кобальта-6О) и линейных ускорителей электронов / 2 Л Изотопная установка для радиационной стерилизации изделий медицинского назначения^";
Установка с облучателем иэ кобальта-60, показанная на рис.1, предназначена для стерилизации пластмассовых изделий одноразового пользования и металлических игл. Данную установку (разработчик ВНИИРТ), находящуюся в стадии строительства, намечается ввести в строй в 1974г.v когда она будет подключена в технологическую линию завода медицинской промышленности.
Принцип действия. Медицинские изделия стерилизуются гамма-излучением кобальта-60. Из совокупности стандартных источников кобальта-60 формируется плоскостной облучатель, ВДОЛЬ которого при облучении непрерывно перемещаются объекты на конвейере. Пуск и управление технологической линией осуществляется дистанционно с пульта управления.
Установка» размещающаяся в двухэтажном здании с КОНСТРУКЦИЯ.
площадью застройки 300 м^ и высотой 7 к, состоит из камеры облучения, облучателя, хранилища облучателя, транспортного конвейера ТП-ЮО, камеры сборки, рабочего стола, контейнера-накопителя, манипулятора М-22, пульта управления.
Камера облучения имеет площадь ~ 100 м* и высоту 3,5 м. Толщина биологической защиты (бетон с р = 2,1 2,3 т/и?)г- 2 м. Мощность экспозиционной дозы за пределами биологической защиты и на выходе из лабиринта не превышает 2,8 р/с (или?,2*10~* А/кг). Лабиринт предназначен для прохода подающей и разгрузочной ветвей кон
– – –
вейера и снабжен дверью с электромеханическим замком. В камере располагаются транспортный конвейер, облучатель и хранилище облучателя.
Облучатель - вертикальная плоскость с габаритами: длина м, высота - 1,06 м, количество стержней - 4 2. Каждый стержень состоит из стальной трубки с источниками излучения и ступенчатой пробки. Верхняя часть облучателя выполнена в виде ступенчатой плиты. С боковых сторон облучателя укреплены ползуны, скользящие по направляющим при перемещении облучателя. Облучатель оборудован системой аварийного сброса источников в хранилище с гидравлическим тормозом. Б конструкции облучателя предусмотрена возможность периодического пополнения облучателя источниками кобальта-60 с целью поддержания требуемой производительности в течение всего срока амортизации установки (Т а м = 10 лет).
Хранилище облучателя выполнено в виде прямоугольной ступенчатой щели в полу камеры облучения и оборудовано защитным тепловым экраном в виде стального блока со змеевиковым теплообменником для охлаждения источников и бетона хранилища.
Для гранспортировашш продукции используется конвейер ТП-ЮО, состоящий из прямых и поворотных секций. Конвейерная линия расположена в 4 ряда относительно плоскости облучателя (по 2 ряда с каждой стороны). Тара с медицинскими объектами облучения расположена в 3 яруса (по высоте) в подвесах, которые перемещаются толкающей цепью со скоростью 10 м/мин.
Камера сборки, предназначенная для загрузки и разгрузки облучателя, размещена над камерой облучения и имеет размеры 4x5x3,5 м.
Стены, пол и потолок выполнены из бетона, являющегося биологической защитой. Камера оборудована смотровым окном и в ней располагаются рабочий стол, контейнер-накопитель и манипулятор м-22.
– – –
В технологическую линию входят: линейный ускоритель электронов, камера облучения» транспортное устройство, система автоматики и защитной блокировки, пульт управления и контроля.
Для осуществления радиационной стерилизации в промышленном масштабе разработан односекционный линейный ускоритель ЛУЗ-8/5В (см. рис.4), обладающий более узкими возможностями в части изменения параметров пучка ускоренных электронов, но зато более простой по конструкции, более надежный в эксплуатации и менее дорогой / 7 * 8 Л Вертикальная компоновка ускоряющей системы в блока излучателя позволяет обходиться без поворотного магнита при установке ускорителя над горизонтальной конвейерной линией промышленного предприятия.
Устойчивость работы ускорителя обеспечивается стабилизацией питающего напряжения (с точностью ±1%) и температуры ускоряющей системы и СВЧ-генератора (с точностью ±1°С). Режимы работы от включения к включению воспроизводятся с точностью до ±2,5% без какихлибо дополнительных подстроек.
Пучок ускоренных электронов выводится наружу через алюминичвую или титановую фольгу после рассеивания его в полосу путем сканирования с частотой от 0,5 до 2 гц отклоняющим магнитом. Размер поля облучения на расстоянии 200 мм от фольги представляет собой полосу длиной 500 мм и шириной 30 мм. Неравномерность плотности потока электронов по длине полосы при сканировании пучка не превышает ±5%.
Пуск и управление технологической линией осуществляются дистанционно с пульта управления.
Камера облучения площадью 120 иг и высотой ~ 9,5 и представляет собой защитный беюнный блок с лабиринтными устройствами для подачи и выгрузки продукции. Она спроектирозана таким образом, что
Рио. 4, Анвйвнй уокорихежь электронов ЛУЭ-8/5В. - 70 -
поступающие на стерилизацию и стерилизованные потоки продукции изолированы друг от друга. Толщина биологической защиты (бетон с р - 2Д * 2,3 т/м 3) - 2,8 м. Мощность экспозиционной дозы за пределами биологической защиты и на выходе из лабиринтик* устройств не превышает 2,8 р/с (иди 7,2-10"^ А/кг). В камере располагаются линейный ускоритель электронов, транспортное устройство, площадки обслуживания. Вход в камеру и обслуживание ускорителя и транспортного устройства осуществляются с первого и второго этажей по лабиринтам. На зходе в лабиринтные устройства установлены двери, имеющие электромеханический замок и блокировку по питанию ускорителя.
Транспортное устройство предназначено для перемещения стерилизуемой продукции с позиции загрузки на облучение и далее на позицию разгрузки W. Оно выполнено в виде четырех конвейеров - подающего, собирающего, лучевого, разгрузочного - последовательно расположенных в горизонтальной плоскости на высоте 0,8 и от пола. Ширина движущихся частей конвейеров равна максимальной ширине развертывающего устройства ускорителя. Подающий и разгрузочный конвейеры представляют собой роликовый транспортер, состоящий из прямых и поворотных секций. Роликовый транспортер позволяет надежно перемещать блочные объекты как по прямолинейным, так и криволинейным участкам при проходе через лабиринтные устройства* Собирающий конвейер выполняет роль накопителя продукции и предназначен для непрерывного литания "лучевого конвейера п. Основным звеном всего транспортного устройства является "лучевой" конвейер (находящийся в зоне облучения), который представляет собой транспортер с металлической сеткой. Все движущиеся части транспортного устройства выполнены из нержавеющей стала, а лучевой конвейер полностью изготовлен из стали XI8HI0T, включая и транспортную ленту, и н о е конструктивное решение удорожав* стоимость аздезшя, но позволяет
71 обеспечить надежную работу в условиях, где имеется мощный источник ионизирующего излучения и поэтому предъявляется повышенные требования к радиационной стойкости материалов. Все конвейеры кинематически связаны между собой и приводятся в движение от одного привода (установленного за пределами камеры облучения. Мощность привода - 1,3 квт.
Скорость движения сетки ленточного транспортера стабилизирована с точностью не хуже ±2% и может регулироваться в пределах 0,003*3 см/сек. Номинальная скорость перемещения продукции при минимальной стерилизующей дозе 2,5 Мрад составляет 0,8 см/сек.
Установка оборудована контрольно-измерительной, защитной, сигнализирующей и дозиметрической аппаратурой, позволяющей осуществлять коагрель основных параметров установки и обеспечить безопасность работы на ней. Для визуального наблюдения за всем процессом радиационной стерилизации установлена телевизионная установка. Контроль и управление производятся из операторского помещения, где установлен пульт управления.
Технические и эксплуатационные характеристики:
Источник излучения - линейный ускоритель электронов ЛУЭ-8/5Б.
Номинальная энергия ускоренных электронов, Иэв...... 8-10 Мощность пучка ускоренных электронов в номинальном режиме, квт 5 Производительность одной технологической линии при дозе I Мрад и плотности облучаемых объектов 0,15*0,2 г/см 3, т/ч 0,9 Интегральная поглощенная доза, дж/кг 2,5*10* (Мрад) (2,5) Неравномерность поглощенной дозы, % ±25
– – –
чем это практикуется за рубежом. Эхи отличия - следствия того, что в нашей стране создаются специализированные радиационно-технояогические установки, впервые встраиваемые в технологические линии конкретных промышленных предприятий (а не центры по стерилизации медицинских и других изделий, существующие независимо от соответствующей промышленности). Именно в случае первых разработок (т. е.
специализированных радиационно-технологических установок) потенциально достижимым является наиболее высокий уровень технико-экономических показателей **", Анализ и составление информации об отечественных и зарубежных разработках установок для радиационной стерилизации показывает, что отечественные разработки по научно-техническому уровню не уступают зарубежным, а по некоторым показателям превосходят (величина коэффициента использования излучения, реализация дозагрузок и д р.).
Представляется целесообразным долгосрочное координирование усилий стран-членов СЭВ (как в рамках сотрудничества по линии КНТС-РТ, так и на двухсторонней основе) в накоплении и развитии коллективного опыта по проблеме радиационной стерилизация медицинс к и гзделий в интересах плодотворного научно-технического и практического решения данной проблемы.
ЛИТЕРАТУРА:
1. мощная радиационная техника. Под ред. С.Джефферсона. Перев.
с англ.* I.., Атомиздат (1967).
2. Фаулер 8*8. Новейшие достижения в области применения изотопов и излучений в США. Доклад Р/540 на 1У Женевской конференции (1971).
3. Пюиг I. P. и др. Развитие радиационного производства во Франции.
Доклад Р/бЗб на 1У Женевской конференции (1971).
^. Протокол 19-го заседания Постоянной Комиссии СЭВ по использованию атомной энергии в мирных целях (часть Ш, приложения 5 и б), Москва (1970).
5. Временные технические требования к исследовательским, многоцелевым и специализированным установкам для радиационных процессов.
Приложение 5 к протоколу третьего заседания КНТС-РТ (1972).
6. Коньков Н.Г. и др. Стерилизация медицинских изделий из полимерных материалов с помощью линейного ускорителя электронов. В с б.
"Радиационная техника". Вып. б, Ы«, Атомиздат (1971) 186.
7. Николаев B.U. Линейные ускорители электронов для стерилизации и радиационной химии. Доклад на Всесоюзном шучно-техническом совещании по использованию ускорителей в народном хозяйстве и медицине". Ленинград, февраль 1971.
8* "Linear Electron Accelerators for Sterilization and Badiation Chemistry. International Buclear Industries Pair Buclex 69 § Oct. 1969.
9. Вавюшшн Б.К. и д р. Устройство для транспортировки блочных объектов к месту облучения их пучком ускоренных электронов.
Доклад на Всесоюзном научно-техническом совещании по использованию ускорителей в народном хозяйстве и медицине. Ленинград,
Начало осваиванию радиационной стерилизации было положено около 15 лет назад. Ученые обнаружили, что существующие на тот момент методики обеззараживания и консервирования продуктов питания ухудшают состояние озонового слоя планеты. Был разработан новый способ - обработка гамма-лучами и ускоренными электронами.
Этот метод оказался гораздо эффективнее - продукты питания дольше оставались пригодными к употреблению. В течение длительного времени сохранялся прежним их внешний вид и вкусовые свойства. Методика была одобрена представителями Всемирной организации здравоохранения. Теперь радиационная стерилизация осуществляется в около семидесяти государств мира.
Согласно статистическим данным, собранным участниками Международной радиационной ассоциации, европейские страны каждый год отправляют на рынок более 200 тыс. тонн облученных продуктов питания. Для большинства товаров разработан оптимальный режим обработки гамма-лучами. Проведено исследование их безвредности и пригодности к употреблению.
Использование радиационной стерилизации в медицине
Гамма-излучение получает все более широкое распространение в качестве методики обеззараживания перевязочных материалов, медикаментов, хирургических инструментов. Применяется оно и для фармацевтических сывороток, продуктов питания и пр. Этот способ относится к числу холодных стерилизаций, так как температура облучаемого объекта поднимается незначительно.В такой промышленной отрасли используются специальные установки, эксплуатация которых производится в строгом соответствии с инструкциями. Когда необходима стерилизация в солидных масштабах, создаются конвейеры. Материалы обрабатывают в упакованном виде.
На предприятиях устанавливаются ускорители электронов и гамма установки. В процессе прохождения электронов сквозь вещество большая доля их энергии тратится на ионизацию. В результате осуществляется уничтожение микроорганизмов. Уровень вирусов и болезнетворных бактерий сокращается пропорционально количеству использованной энергии электронов.
Преимущества радиационной стерилизации перед газовой
Товары обрабатываются, будучи помещенными в герметичные упаковки. Благодаря этому увеличиваются сроки их хранения. Приступать к использованию продукции можно непосредственно после облучения.В области эксплуатации облучающей установки не создаются сопутствующие вредные вещества. Стерилизованные гамма-лучами изделия остаются сухими и не содержат канцерогенных составляющих.
В нашем сознании прочно укрепилось понимание, что техногенная радиация опасна для здоровья. Но так ли это на самом деле? Об этом не принято широко говорить, но энергия атома активно используется во многих промышленных отраслях. И не только для получения дешевой электроэнергии! Сегодня в 60 странах мира немалая часть пищевых и сельскохозяйственных продуктов стерилизуется с помощью радиации, а полимеры для покрышек и электрических проводов упрочняются на электронных облучателях.
В чем суть технологии?
В основе радиационной технологии лежит использование энергии ионизирующего излучения, образующегося при распаде изотопов радиоактивного элемента или при бомбардировке вещества ускоренными электронами. Проникая внутрь живого микроорганизма, бета- и гамма-частицы убивают вредные патогенные микроорганизмы, инициируют протекание определенных химических реакций, подавляют биологические процессы в пищевых продуктах и изменяют физико-химические свойства полимерных материалов.
При этом ни один из видов ионизирующего облучения не делает опасными обрабатываемые продукты и материалы. Поэтому радиационная технология успешно применяется при проведении нескольких технологических процессов:
- стерилизации;
- структурирования;
- отверждения и прививки.
В качестве радиационных облучателей применяются источники γ-излучения от изотопов цезия-137 и кобальта-60, рентгеновское излучение от установок с энергией менее 5 мегавольт, пучки электронов высокой активности, генерируемых электронными ускорителями в интервале энергий до 10 мегавольт.
Несмотря на то, что Россия первой использовала ионизирующее облучение для дезинфекции посевов (в 1958 году посевное зерно и картофель, ввозимые из Канады и загрязненные долгоносиком, были обработаны на ионизирующих облучателях), технология не нашла широкого применения в нашей стране. Наибольшее количество облучателей расположено в Китае (40%) и США (39%), в России лишь планируется создать один центр по радиационной обработке. Только с 1 января 2016 года заработал ГОСТ ISO 14470-2014, разрешающий стерилизовать пищевые продукты электронными и ионизирующими облучателями, но до сих пор ГОСТы для конкретных продуктов не разработаны.
Интересный факт
По данным ФАО ООН, в Европе ежегодно изготавливается и реализуется свыше 200 тысяч тонн продуктов, простерилизованных облучателями. В Канаде радиацией обеззараживают замороженных цыплят, в Нидерландах - устрицы и лягушачьи лапки. В Австралии с 1979 года облучают замороженных креветок в промышленных масштабах. В США каждый год с помощью радиации стерилизуется свыше 100 миллионов килограммов пищевых продуктов, среди которых: мясо (фарш), овощи,фрукты, какао, кофе, яйца, овсяные хлопья, пиво, консервы, приправы и сгущенное молоко.
Сферы использования радиационного облучения
- Производство автомобильных покрышек для колес.
Крупные изготовители автомобильных покрышек США, Франции и Японии применяют радиацию для структурирования невулканизированной резины (радиационную вулканизацию). При этом улучшаются ее механические свойства, повышается усталостная прочность и износостойкость.
- Упрочнение телефонных кабелей.
С помощью радиации обрабатываются полимеры, идущие на изготовление изоляции для проводов и кабелей. После облучения оболочка приобретает два важных качества: не «течет» при повышенной температуре и при увеличении порога температуры плавления приобретает свойство резины. Такие изоляционные характеристики важны при обустройстве внутренних электрических схем звукового и электронного оборудования, линий электропередач, а также востребованы в авиационной, автомобильной, и судостроительной промышленности. К сожалению, радиационная технология не применима к кабелям высокого напряжения, поскольку ограничивается проникновение электронов. Поэтому многие ведущие концерны, специализирующиеся на выпуске проводов и кабелей, помимо облучателей используют линии химического структурирования.
- Дезинсекция зерна
В основе многих методов по очистке зерна лежит использование стерилизующего эффекта γ-излучения (радиационная дезинсекция). Большинство насекомых-вредителей после облучения дозой 100-200 Гр становятся стерильными и спустя 2-3 недели погибают. Качество риса, кукурузы, пшеницы, гречихи и другого зерна не ухудшается, облучение частично защищает зерновые запасы от повторного заражения, поскольку при спаривании со стерильными самками, которые еще могут остаться живыми, плодовитость особей резко падает.
- Стерилизация кормов для животных
Технология радиационной обработки кормов и кормовых добавок для животных развита во многих странах, особенно в Израиле, и считается достойной альтернативной пропионовой кислоте. Высокие дозы γ-облучения применяются при получении кормов для лабораторных животных, а низкие дозы - для сельскохозяйственных животных. В процессе обработки продукция быстро и надежно очищается от сальмонеллы, трихинелл и других патогенных микроорганизмов.
- Дезинфекции и стерилизации медицинских изделий
Радиационная стерилизация медицинских изделий на промышленном уровне начала использоваться в 50-60-х годах во Франции, США, Австралии и Великобритании. И дело не только в том, что метод позволяет быстро обеззараживать немалые партии шприцов, катетеров и наборов для переливания крови, а то, что изделия могут стерилизоваться в упаковках, в результате чего успешно решается проблема повторного загрязнения.
Свою эффективность доказала радиационная обработка медицинской одежды, изготовленной из нетканого пластического материала, - бахил, салфеток, наборов для операций, хирургических костюмов. В сравнении с альтернативным методом, в процессе которого используется специальный газ, уровень стерильности после облучения впечатляет - 106 КОЕ (1 бактерия) на миллион изделий. При этом не нужно держать изделия в нагретом виде восемь часов и постоянно вентилировать производственное помещение, где проводится дезинфекция.
- Пищевое производство
После того, как выяснилось, что стерилизация сернистым газом овощей и фруктов вредит озоновому слою и нарушает экологическое равновесие, технология лучевой обработки пищевых продуктов гамма-облучением стала использоваться во всем мире. Поскольку эффект стерилизации достигается при обычной температуре воздуха и не приводит к нагреву продуктов, способствуя сохранению их свежести, ее назвали холодной пастеризацией. Технология успешно применяется для различных целей:
Многие страны накопили многолетний опыт безопасного использования радиационной обработки свыше 68 видов пищевых и сельскохозяйственных продуктов. В Америке и Европе ее применяют в промышленных масштабах на протяжении последних десятилетий.В основном, с целью консервации и продления срока хранения облучают полуфабрикаты, мясо, рыбу, морепродукты, картофель, концентраты фруктовых соков, ягоды и фрукты в весенне-летнее время.
Ионизирующее излучение подавляет прорастание клубней и луковиц. Воздействуя на обменные процессы, радиация увеличивает время хранения до одного года и более при температуре воздуха 6-8 градусов. При этом радиация воздействует на кожуру корнеплодов, не затрагивая запасающие ткани, сохраняя как их вкус, так питательную ценность.
Международная маркировка облученных продуктов
Чтобы потребители могли выбрать между облученным и необлученным продуктом, во многих странах была принята международная маркировка продуктов, обработанных ионизирующим излучением, - логотип «Radura-logo» (радура). В некоторых государствах логотипы на этикетках пищевых продуктов сопровождаются дополнительными надписями:«Treated with ionizing energy», «Treated by irradiation» или «Treated with radiation»(обработано радиацией), или надписи заменяют знак.
Радиоактивная пастеризация: безопасна или нет?
Споры о безопасности или вредоносности радиоактивной обработки продуктов были прекращены в 1980 году. Сразу три авторитетные организации: МАГАТЭ, ВОЗ и ООН на основании анализа результатов многочисленных исследований, сделали заключение о безопасности пищевой продукции для человека, облученной дозой до 10 кГр.
Советские ученые института питания АМН СССР в ходе опытов, в процессе которых собакам полтора года скармливалось мясо, облученное дозами радиации 0,6-0,8 мРад, неблагоприятных влияний не выявили. Аналогичные эксперименты с мышами, крысами, собаками и обезьянами проводились 30 исследовательскими лабораториями Америки. Пищевые продукты питания (21 вид), обработанные дозам 2,8 мРад и 5,58 мРад, давались подопытным животным в течение продолжительного времени, в результате чего отклонений в их здоровье ученые не обнаружили. Исследования на добровольцах, кратковременно питавшихся обработанной радиацией пищей, также не выявили опасных свойств у использованных продуктов, подвергшихся γ-облучению, и их отрицательного воздействия на организм человека.
Таким образом, было доказано, что продукты питания после облучения не меняют вкусовых и питательных качеств, не оказывают негативного влияния на здоровье и репродуктивную систему человека. С одной лишь поправкой - доза гамма-излучения не должна превышать установленные нормативы, иначе лучевая обработка приведет к накоплению радионуклидов в пище.
Сегодня появились новые сведения о том, что радиоактивная пастеризация вызывает образование свободных радикалов, которые относятся к мутагенам и канцерогенам. Но, как свидетельствуют проведенные исследования, их доля мала и не превышает количества, образующегося при обычной обработке продуктов.
Радиационное облучение: перспективы на будущее
Поскольку холодная пастеризация удешевляет продукцию консервной промышленности и позволяет вместо металлических банок использовать пластиковые контейнеры, с ее помощью можно получать мясные и колбасные изделия, упакованные в герметичную пленку и способные сохраняться до 3-х месяцев при обычных температурах.
За счет химической привязки активных веществ к фиксированной среде, с помощью радиационного облучения можно получать ферменты и лекарства, которые способны поддерживать высокую активность в течение долгого времени и, таким образом, иметь более длительный срок хранения.
Не менее актуально использование гамма-облучения в синтезе биологически активных полимеров, которые могут применяться при производстве имплантатов и медицинских устройств, рассчитанных на длительный контакт с тканями.
Кроме того, проведены успешные эксперименты в США и Германии по радиационной очистке сточных вод и использования отстоя в качестве удобрения или корма для жвачных животных. Полученные кормовые добавки были полностью очищены от возбудителей инвазивных и инфекционных заболеваний, не обладали токсичным действием.
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ОБЩАЯ ФАРМАКОПЕЙНАЯ СТАТЬЯ
Стерилизация ОФС.1.1.0016.15
Взамен ст. ГФ XI , вып.2
Настоящая общая фармакопейная статья устанавливает методы и условия стерилизации, используемые при получении стерильных лекарственных средств.
Под стерильностью понимают отсутствие жизнеспособных микроорганизмов и их спор.
Стерилизация – это валидируемый процесс, используемый при получении стерильных лекарственных форм для освобождения продукта, оборудования, вспомогательных веществ и упаковки от живых микроорганизмов и их спор.
При изменении условий стерилизации, в том числе при изменении объема загрузки стерилизатора, необходимо проводить повторную валидацию.
Методы, описанные ниже, применимы для инактивации бактерий, дрожжевых и плесневых грибов.
По возможности продукцию стерилизуют в конечной упаковке (финишная стерилизация).
В случаях, когда финишная стерилизация невозможна, используют метод мембранной фильтрации или получение лекарственных препаратов в асептических условиях без последующей стерилизации конечного продукта. Дополнительно возможно проводить обработку объекта (например, стерилизация гамма-излучением) в конечной упаковке. Во всех случаях упаковка и укупорочные средства должны обеспечивать стерильность препарата в течение всего срока годности.
УРОВЕНЬ ОБЕСПЕЧЕНИЯ СТЕРИЛЬНОСТИ
Для методов, описанных ниже, в случае необходимости, указывают уровень обеспечения стерильности (УОС).
Уровень обеспечения стерильности процесса стерилизации – это степень гарантии, с которой процесс обеспечивает стерильность всех единиц продукции в серии. Для конкретного процесса уровень обеспечения стерильности определяется как вероятность наличия нестерильной единицы в серии. Например, УОС = 10 −6 означает, что в подвергнутой стерилизации серии готового продукта объемом 10 6 единиц существует вероятность наличия не более одного жизнеспособного микроорганизма. Уровень обеспечения стерильности процесса стерилизации для конкретного продукта устанавливают в процессе валидации.
МЕТОДЫ И УСЛОВИЯ СТЕРИЛИЗАЦИИ
Стерилизация может быть проведена одним из следующих методов или их комбинацией.
- Термические методы:
- насыщенным водяным паром под давлением (автоклавирование);
- горячим воздухом (воздушная стерилизация).
- Химические методы:
- газами;
- растворами антисептиков.
- Стерилизация фильтрованием (через фильтры с требуемым размером пор).
- Радиационный метод стерилизации.
Использование модификации или комбинации этих методов допускается при условии проведения валидации выбранного процесса стерилизации, чтобы обеспечить как эффективность процесса, так и целостность продукта, упаковки и укупорочных средств.
Для всех методов стерилизации, в том числе при использовании стандартных условий, для подтверждения обеспечения необходимых условий стерилизации всей серии продукта, на протяжении всего процесса стерилизации проводят мониторинг на критических стадиях производства.
Термическая стерилизация
Стерилизация насыщенным паром под давлением (автоклавирование)
Стерилизацию насыщенным паром осуществляют при температуре
120 – 122°С под давлением 120 кПа и при температуре 130 – 132 °С под давлением 200 кПа. Этот метод чаще всего применяют для водных растворов и других жидких лекарственных форм в герметично укупоренных, предварительно простерилизованных флаконах, ампулах или других видах упаковки. Стерилизацию проводят в паровых стерилизаторах (автоклавах). Стандартными условиями являются нагревание при температуре 120 – 122 °С в течение 8–15 мин. Время стерилизации зависит от физико-химических свойств и объема продукта, а также используемого оборудования (табл. 1).
Таблица 1 — Время стерилизации для различного объема раствора
Жиры и масла стерилизуют при температуре 120 – 122 °С в течение 2 ч.
Изделия из стекла, фарфора, металла, перевязочные и вспомогательные материалы, при необходимости санитарную технологическую одежду, стерилизуют при температуре 120 – 122 °С – в течение 45 мин, при
130 – 132 °С – в течение 20 мин. Для стерилизации изделий из резины следует использовать первый из указанных режимов.
Допускаются другие сочетания времени и температуры, если предварительно доказано, что выбранный режим стерилизации обеспечивает необходимый и воспроизводимый уровень гибели микроорганизмов. Используемые процедуры должны обеспечивать уровень обеспечения стерильности не более 10 -6 .
Автоклав загружают таким образом, чтобы обеспечить однородность температуры в пределах всей загрузки. В процессе автоклавирования следует регистрировать условия процесса стерилизации (температуру, давление и время). Температуру, как правило, измеряют с помощью термочувствительных элементов, помещенных в контрольные упаковки, вместе с дополнительными термоэлементами, помещенными в самые низкотемпературные места стерилизационной камеры, которые устанавливаются заранее. Условия каждого цикла стерилизации регистрируются, например, в виде температурно-временной диаграммы или другим подходящим способом.
Для оценки эффективности каждого цикла стерилизации возможно использование как химических (термовременных), так и биологических индикаторов.
Стерилизация горячим воздухом (воздушная стерилизация)
Для этого метода термической стерилизации стандартными условиями являются нагревание при температуре не менее 160 °С в течение не менее
2 ч.
Для стерилизации термостойких порошкообразных веществ (натрия хлорида, цинка оксида, талька, белой глины и др.) или минеральных и растительных масел, жиров, ланолина, вазелина, воска и др. температуру и время стерилизации устанавливают в зависимости от массы образца (табл. 2 и 3).
Таблица 2 — Условия стерилизации для термостойких порошкообразных веществ
Таблица 3 — Условия стерилизации для минеральных и растительных масел, жиров, ланолина, вазелина, воска и др.
Изделия из стекла, металла, фарфора, установки для стерилизующего фильтрования с фильтрами и приемники фильтрата стерилизуют при температуре 180 °С в течение 60 мин, или при температуре 160 °С – в течение 2,5 ч.
Воздушную стерилизацию при температуре более 220 °С обычно применяют для стерилизации и депирогенизации стеклянной упаковки. В этом случае должно быть доказано уменьшение на 3 порядка количества термостойких эндотоксинов вместо использования биологических индикаторов.
Допускается использование сочетаний времени и температуры, если предварительно доказано, что выбранный режим стерилизации обеспечивает необходимый и воспроизводимый уровень гибели микроорганизмов. Используемые процедуры должны обеспечивать уровень обеспечения стерильности не более 10 -6 .
Воздушную стерилизацию проводят в специальном сухожаровом шкафу с принудительной циркуляцией стерильного воздуха или на другом оборудовании, специально предназначенном для этих целей. Стерилизационный шкаф загружают таким образом, чтобы обеспечить однородность температуры в пределах всей загрузки. Температуру в стерилизационном шкафу, как правило, измеряют с помощью термочувствительных элементов, помещенных в контрольные упаковки, вместе с дополнительными термоэлементами, помещенными в самые низкотемпературные места стерилизационного шкафа, которые устанавливаются заранее. В ходе каждого цикла стерилизации регистрируют температуру и время. Для оценки эффективности каждого цикла стерилизации возможно использование как химических (термовременных), так и биологических индикаторов.
Химическая стерилизация
Химическую стерилизацию проводят газом или растворами.
Газовая стерилизация
Стерилизация газом применяется только в случае, если не могут быть использованы другие методы. При этом способе стерилизации должно быть обеспечено проникновение газа и влаги в стерилизуемый продукт, а также последующая дегазация и удаление продуктов его разложения в стерилизуемом продукте до уровня, не вызывающего токсического эффекта при применении лекарственного средства.
Стерилизацию газом проводят в газовых стерилизаторах или микроанаэростатах (портативный аппарат), оборудованных системой подачи газа и постстерилизационной дегазации. В качестве газа обычно используют оксид этилена. В связи с его высокой пожароопасностью, допускается его смешивание с каким-либо инертным газом.
Стерилизацию газом проводят при следующих режимах:
- – оксид этилена: стерилизующая доза 1200 мг/дм 3 , температура не менее
18 °С, относительная влажность 80 %, время выдержки – 16 ч (портативный аппарат); - – смесь оксида этилена и бромистого метила (1:2,5):
а) стерилизующая доза 2000 мг/дм 3 , температура 55 °С, относительная влажность 80 %, время выдержки 4 ч;
б) стерилизующая доза 2000 мг/дм 3 , температура не менее 18 °С, относительная влажность 80 %, время выдержки 16 ч.
Допускается использование других валидированных режимов газовой стерилизации, обеспечивающих стерильность и сохранность объекта.
Оксид этилена может проявлять мутагенные свойства и токсичность, особенно при использовании материалов, содержащих ионы хлора. В связи с токсичностью оксида этилена и бромистого метила применение стерилизованных этими газами изделий допускается только после их дегазации, т. е. выдержки в вентилируемом помещении до допустимых остаточных количеств, указанных в нормативной документации.
Условия дегазации зависят от назначения, способа применения, размеров изделий, материала изделия и упаковки и указываются в нормативно-технической документации на изделие.
По возможности в процессе стерилизации регистрируют следующие показатели: концентрацию газа, относительную влажность, температуру и время стерилизации. Измерения проводят в тех зонах, где условия стерилизации достигаются хуже всего, что устанавливают в процессе валидации.
Стерилизуемые изделия упаковывают в пакеты из полиэтиленовой пленки толщиной от 0,06 до 0,20 мм, пергамента и др. Метод рекомендован для изделий из резины, полимерных материалов, стекла, металла.
Эффективность процесса газовой стерилизации проверяют при каждой загрузке с помощью биологических индикаторов.
Перед выпуском каждой серии проверяют стерильность на определенном количестве образцов.
Химическая стерилизация растворами
Химическую стерилизацию проводят растворами антисептиков (водорода пероксид и надкислоты). Эффективность стерилизации растворами антисептиков зависит от концентрации активно действующего вещества, времени стерилизации и температуры стерилизующего раствора.
При стерилизации 6 % раствором водорода пероксида температура стерилизующего раствора должна быть не менее 18 °С, время стерилизации – 6 ч; при температуре 50 °С – 3 ч.
При стерилизации 1 % раствором дезоксона-1 (по надуксусной кислоте) температура стерилизующего раствора должна быть не менее 18 °С, время стерилизации 45 мин.
Химическую стерилизацию растворами антисептиков проводят в закрытых емкостях из стекла, пластмассы или емкостях, покрытых неповрежденной эмалью, при полном погружении изделия в раствор на время стерилизации. После этого изделие промывают стерильной водой в асептических условиях.
Метод стерилизации растворами антисептиков применяют для изделий из полимерных материалов, резины, стекла, коррозийно-стойких металлов.
Стерилизация фильтрованием
Некоторые действующие вещества и лекарственные препараты, которые не могут быть подвергнуты финишной стерилизации ни одним из описанных выше методов, могут быть простерилизованы с использованием мембранных фильтров. Такие продукты требуют соблюдения специальных мер предосторожности. Производственный процесс и производственная среда должны обеспечивать минимальный риск микробного загрязнения и требуют регулярного мониторинга. Оборудование, упаковка, укупорочные средства и, по возможности, ингредиенты следует подвергать соответствующей стерилизации. Рекомендуется проводить фильтрацию непосредственно перед наполнением упаковки. Операции, следующие за фильтрацией, проводят в асептических условиях.
Предварительную фильтрацию осуществляют через мембранные фильтры с размером пор не более 0,45 мкм. Затем растворы пропускают через мембранные фильтры с номинальным размером пор не более 0,22 мкм, способные задерживать не менее 10 7 микроорганизмов Pseudomonas diminuta на квадратный сантиметр поверхности. Допускается использование других типов фильтров, обеспечивающих такую же эффективность фильтрации.
Пригодность мембранных фильтров устанавливают путем микробиологических испытаний с использованием соответствующих микроорганизмов, например, Pseudomonas diminuta (ATCC 19146, NCIMB 11091 или CIP 103020). Рекомендуется использовать не менее 10 7 КОЕ/см 2 активной поверхности фильтра. Суспензия микроорганизмов должна быть приготовлена в триптонно-соевом бульоне, который после прохождения через фильтр собирают асептически и инкубируют в аэробных условиях при температуре не более 32 °С.
Уровень фильтрации определяют как величину логарифма снижения (ВЛС) микробной загрязненности. Например, если при фильтрации через мембранный фильтр с размером пор 0,22 мкм задерживается 107 микроорганизмов, ВЛС составляет не менее 7.
Следует учитывать уровень микробной контаминации до начала фильтрации, пропускную способность фильтра, объем серии продукта, продолжительность фильтрации, а также избегать загрязнений продукта микроорганизмами с фильтра. Срок использования фильтра не должен превышать времени, установленного при валидации данного фильтра в сочетании с конкретным фильтруемым продуктом. Не следует повторно использовать мембранные фильтры.
Целостность готового к применению мембранного фильтра проверяют до и после фильтрации путем испытаний, соответствующих типу фильтра и стадии проверки, например, испытанием на определение насыщенности («точка пузырька») методом диффузионного потока или выдержкой под давлением.
В связи с тем, что при проведении стерилизации фильтрованием существует больший потенциальный риск по сравнению с другими методами стерилизации, рекомендуется проводить предварительную фильтрацию через мембранные фильтры в тех случаях, когда низкий уровень микробной контаминации не может быть обеспечен другими средствами.
Получение лекарственных препаратов в асептических условиях без последующей стерилизации конечного продукта
Целью получения лекарственных препаратов в асептических условиях без последующей стерилизации конечного продукта является сохранение стерильности препарата с использованием компонентов, каждый из которых был предварительно простерилизован одним из вышеописанных методов. Это достигается путем проведения процесса в помещениях определенного класса чистоты, а также использования условий и оборудования, обеспечивающих стерильность.
В асептических условиях могут осуществляться: процесс наполнения упаковки, укупорка, асептическое смешивание ингредиентов с последующим асептическим наполнением и укупоркой. Для сохранения стерильности ингредиентов и готового продукта в ходе производственного процесса особое внимание следует уделять:
- – состоянию производственной среды;
- – персоналу;
- – критическим поверхностям;
- – стерилизации упаковки и укупорочных средств и передаточным процедурам;
- – предельно допустимому времени хранения продукта до момента наполнения конечной упаковки.
Валидация процесса включает надлежащую проверку всех перечисленного выше пунктов, а также систематический контроль с применением имитационных тестов с использованием питательной среды, которую инкубируют и исследуют на наличие микробной контаминации (тесты на заполнение питательными средами). Перед выпуском каждой серии продукта, простерилизованного фильтрованием и/или изготовленного в асептических условиях, следует проводить испытания стерильности на соответствующем количестве образцов.
Радиационный метод стерилизации
Радиационный метод стерилизации осуществляют путем облучения продукта ионизирующим излучением. Данный метод может быть использован для стерилизации лекарственного растительного сырья, лекарственных растительных препаратов, лекарственных средств растительного происхождения и др.
γ-излучение, источником которого может быть либо радиоизотопный элемент (например, кобальт-60), либо пучок электронов, подаваемый соответствующим ускорителем электронов.
Для этого метода стерилизации дозу поглощения устанавливают от
10 до 50 кГр. Допускается использование других доз, если предварительно доказано, что выбранный режим обеспечивает необходимый и воспроизводимый уровень летальности микроорганизмов. Используемые процедуры и меры предосторожности должны обеспечивать уровень обеспечения стерильности не более 10 -6 .
Преимуществом радиационной стерилизации является ее низкая химическая активность и легко контролируемая доза излучения, которая может быть точно измерена. Радиационная стерилизация проходит при минимальной температуре, однако могут быть ограничения при использовании некоторых типов стеклянной и пластиковой упаковки.
В процессе радиационной стерилизации следует постоянно осуществлять мониторинг поглощенного готовым продуктом излучения при помощи установленных дозиметрических методов независимо от величины дозы. Дозиметры калибруют по отношению к стандартному источнику на эталонной радиационной установке при получении от поставщика и затем с периодичностью, не превышающей одного года.
Если предусмотрена биологическая оценка, ее проводят с использованием биологических индикаторов.
БИОЛОГИЧЕСКИЕ ИНДИКАТОРЫ СТЕРИЛИЗАЦИИ
Биологические индикаторы – это стандартизованные препараты определенных микроорганизмов, используемые для оценки эффективности процесса стерилизации.
Биологический индикатор обычно представляет собой споры бактерий, нанесенные на инертный носитель, например, полоску фильтровальной бумаги, стеклянную пластинку или пластиковую пробирку. Инокулированный носитель изолируют так, чтобы предотвратить его повреждение или загрязнение и, в то же время, обеспечить контакт стерилизующего агента с микроорганизмами. Суспензии спор могут находиться в герметично запаянных ампулах.
Биологические индикаторы готовят таким образом, чтобы обеспечить их сохранность при определенных условиях; для них должен быть указан срок годности.
Те же штаммы бактерий, что используют при производстве биологических индикаторов, могут быть инокулированы непосредственно в жидкий продукт, подлежащий стерилизации, или в жидкий продукт, аналогичный стерилизуемому. В этом случае должно быть доказано, что жидкий продукт не оказывает ингибирующего действия на споры, особенно на их прорастание.
Для биологического индикатора указывают следующие характеристики: вид бактерий, используемых в качестве эталонных микроорганизмов; номер штамма в исходной коллекции; число жизнеспособных спор, приходящееся на носитель; величину D .
Величина D – значение параметра стерилизации (продолжительность или поглощенная доза), обеспечивающее снижение числа жизнеспособных микроорганизмов до 10 % от их исходного числа. Эта величина имеет смысл для строго определенных экспериментальных условий стерилизации. Биологический индикатор должен содержать только указанные микроорганизмы. Допускается использование биологических индикаторов, содержащих более одного вида бактерий на одном носителе. Должна быть указана информация о питательной среде и условиях инкубации.
Рекомендуется размещать индикаторы в областях, наименее доступных для стерилизующего агента, определенных предварительно эмпирически или на основании предварительных физических измерений. После воздействия стерилизующего агента носитель спор переносят на питательную среду в асептических условиях.
Допускается использование биологических индикаторов промышленного производства в закрытых ампулах с питательной средой, помещенных непосредственно в упаковку, защищающую инокулированный носитель.
Выбор эталонных микроорганизмов для биологических индикаторов осуществляют с учетом следующих требований:
- – устойчивость тест-штамма к конкретному методу стерилизации должна быть выше по сравнению с устойчивостью всех патогенных микроорганизмов и других микроорганизмов, контаминирующих продукт;
- – тест-штамм должен быть непатогенным;
- – тест-штамм должен легко культивироваться.
Если после инкубации наблюдается рост эталонных микроорганизмов, это свидетельствует о неудовлетворительно проведенном процессе стерилизации.
Особенности применения биологических индикаторов стерилизации
Стерилизация насыщенным паром под давлением
Биологические индикаторы для контроля стерилизации насыщенным паром под давлением рекомендуется использовать при валидации циклов стерилизации. Рекомендуется использовать Bacillus stearothermophilus (например, ATCC 7953, NCTC 10007, NCIMB 8157 или CIP 52.81). Число жизнеспособных спор должно превышать 5 · 10 5 на носитель. Величина D при температуре 121 °С должна составлять более 1,5 мин. При обработке биологического индикатора паром при температуре (121 ± 1) °С под давлением 120 кПа в течение 6 мин должно наблюдаться сохранение жизнеспособных спор, а обработка при той же температуре в течение 15 мин должна приводить к полной гибели эталонных микроорганизмов.
Воздушная стерилизация
Рекомендуется использовать для приготовления биологических индикаторов Bacillus subtilis (например, var . niger ATCC 9372, NCIMB 8058 или CIP 77.18). Число жизнеспособных спор должно превышать 1 ∙ 10 5 на носитель, величина D при температуре 160 °С составляет 1 – 3 мин. Для стерилизации и депирогенизации стеклянного оборудования часто используют горячий воздух при температуре более 220 °С. В этом случае заменой биологическим индикаторам может служить снижение на 3 порядка количества термостойких бактериальных эндотоксинов.
Радиационная стерилизация
Биологические индикаторы могут использоваться для мониторинга текущих операций в качестве дополнительной оценки эффективности установленной дозы излучения, особенно в случае стерилизации ускоренными электронами. Рекомендуются споры Bacillus pumilus (например, ATCC 27.142, NCTC 10327, NCIMB 10692 или CIP 77.25). Число жизнеспособных спор должно превышать 1 ∙ 10 7 на носитель. Величина D должна составлять более 1,9 кГр. Следует убедиться, что после облучения биологического индикатора дозой 25 кГр (минимальная поглощенная доза) рост эталонных микроорганизмов не наблюдается.
Газовая стерилизация
Использование биологических индикаторов необходимо при проведении всех процедур газовой стерилизации как при валидации циклов, так и при проведении рутинных операций. Рекомендуется использовать споры Bacillus subtilis (например, var . niger ATCC 9372, NCIMB 8058 или CIP 77.18) при использовании этилена оксида. Число жизнеспособных спор должно превышать 5 · 10 5 на носитель. Параметры устойчивости следующие: величина D составляет более 2,5 мин для испытания цикла при концентрации этилена оксида 600 мг/л, температуре 54 °С и 60 % относительной влажности. Следует убедиться, что после 60-минутного цикла стерилизации с указанными параметрами не наблюдается рост эталонных микроорганизмов, тогда как после 15 мин цикла стерилизации при более низкой температуре (600 мг/л, 30 °С, 60 % влажности) жизнеспособность спор сохраняется.
Биологический индикатор должен позволять обнаруживать недостаточную влажность в стерилизаторе и продукте: при воздействии на него этилена оксида концентрации 600 мг/л при температуре 54 °С в течение 60 мин без увлажнения должна сохраняться жизнеспособность спор.